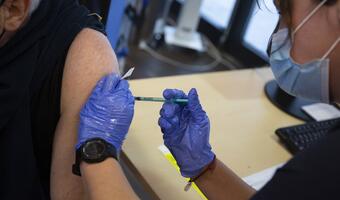
Szczepionka: Nie tylko skuteczna ale i... bezpieczna!
Nad szczepionką przeciwko COVID-19 prowadzone są intensywne badania na całym świecie, opracowywanych jest już ponad 110 preparatów. Jednak taka szczepionka musi być nie tylko skuteczna, ale i bezpieczna - podkreśla dr hab. Aneta Nitsch-Osuch z Warszawskiego Uniwersytetu Medycznego.
AstraZeneca, jedna z firm prowadzących z badaczami Oxford University badania na szczepionką, która ma chronić przed koronawirusem SARS-CoV-2, zapowiedziała, że jeszcze przed zakończeniem badań klinicznych rozpoczyna już jej produkcję. Chodzi o to, by w chwili zakończenia testów można było wykonać jak najszybciej, jak najwięcej szczepień ochronnych.
Firma będzie w stanie udostępnić nawet 2 mld dawek tego preparatu - zapowiedział jej szef Pascal Soriot w rozmowie z BBC. Przyznał, że jest to finansowo ryzykowne, bo w razie niepowodzenia wszystkie preparaty trzeba będzie zutylizować. Według niego warto jest podjąć to ryzyko.
Najbardziej oczekuje się tego, żeby szczepionka, na która czeka cały świat, skutecznie chroniła przed zakażeniem koronawirusami SARS-CoV-2. Mniej się mówi tym, że musi być ona również bezpieczna.
Zwraca na to uwagę dr hab. Aneta Nitsch-Osuch, kierownik Zakładu Medycyny Społecznej i Zdrowia Publicznego Warszawskiego Uniwersytetu Medycznego. „Szczepionka przeciwko COVID-19 musi być nie tylko skuteczna, ale i bezpieczna” - powiedziała podczas konferencji prasowej online „Wirusologia 2020”. Dlatego konieczne jest przeprowadzenie wszystkich niezbędnych badań, w tym badań klinicznych na wielu ochotnikach.
Niezbędne są też długotrwałe obserwacje, żeby wykryć ewentualne późne powikłania szczepionki. Nawet jeśli rzadko będą występować, to przy masowych szczepieniach mogą być one poważnym problemem.
Badania na szczepionkami to skomplikowany i długotrwały proces. „Każda z nich jest poddawana kompleksowym badaniom klinicznym pod względem jakości, skuteczności i bezpieczeństwa. Dopiero po potwierdzeniu bezpieczeństwa i skuteczności przygotowywana jest dokumentacja składana do urzędów rejestracji leków” - wyjaśnia specjalistka.
Badania nad szczepionka przeciwko COVID-19 prowadzone są w wyjątkowo szybkim tempie. Według Światowej Organizacji Zdrowia (WHO), pierwsze partie mogą być dostępne w ekspresowym tempie, bo już za 18 lub 24 miesiące. Zwykle takie prace prowadzone są przez co najmniej 10 lat, sam proces zbierania dokumentacji rejestracyjnej w normalnych warunkach trwa około roku. Trzeba też pamiętać, że część badań kończy się niepowodzeniem.
„Większość badanych preparatów nie wychodzi nawet poza fazę badań przedklinicznych ze względu na brak powodzenia w wykształceniu odpowiedniej reakcji układu odpornościowego. Przyczyny tego mogą być różne, takie jak niewłaściwe dopasowanie dawki preparatu lub brak odpowiedzi organizmu” - tłumaczy dr hab. Aneta Nitsch-Osuch.
Bardzo ważna jest ocena jakości szczepionki, gdyż jest ona poddawana takim samym rygorom, jak rejestracja leków. „Każda seria preparatu przechodzi badania jakościowe, zarówno u producenta, jak i w niezależnym laboratorium państwowym. Jakość szczepionek, które już znajdują się na rynku, monitoruje Inspekcja Farmaceutyczna” - dodaje ekspertka z WUM. Ponadto szczepionki są monitorowane przez długi czas już po wprowadzeniu do masowej produkcji.
Specjaliści twierdzą, że do opracowania i produkcji szczepionki chroniącej przed koronawirusem SARS-CoV-2 wykorzystywane będą nowe technologie, które jednocześnie powinny gwarantować większe ich bezpieczeństwo. Testowane są różnego typu preparaty, w tym szczepionki DNA i RNA, rekombinowane białka wywołujące odpowiednia reakcję odpornościowa, a także czynniki infekcyjne z usuniętymi genami oraz żywe, niepatogenne drobnoustroje przenoszące i eksponujące na swej powierzchni czynniki zakaźne.
PAP/ as/
Dziękujemy za przeczytanie artykułu!
Pamiętaj, możesz oglądać naszą telewizję na wPolsce24. Buduj z nami niezależne media na wesprzyj.wpolsce24.